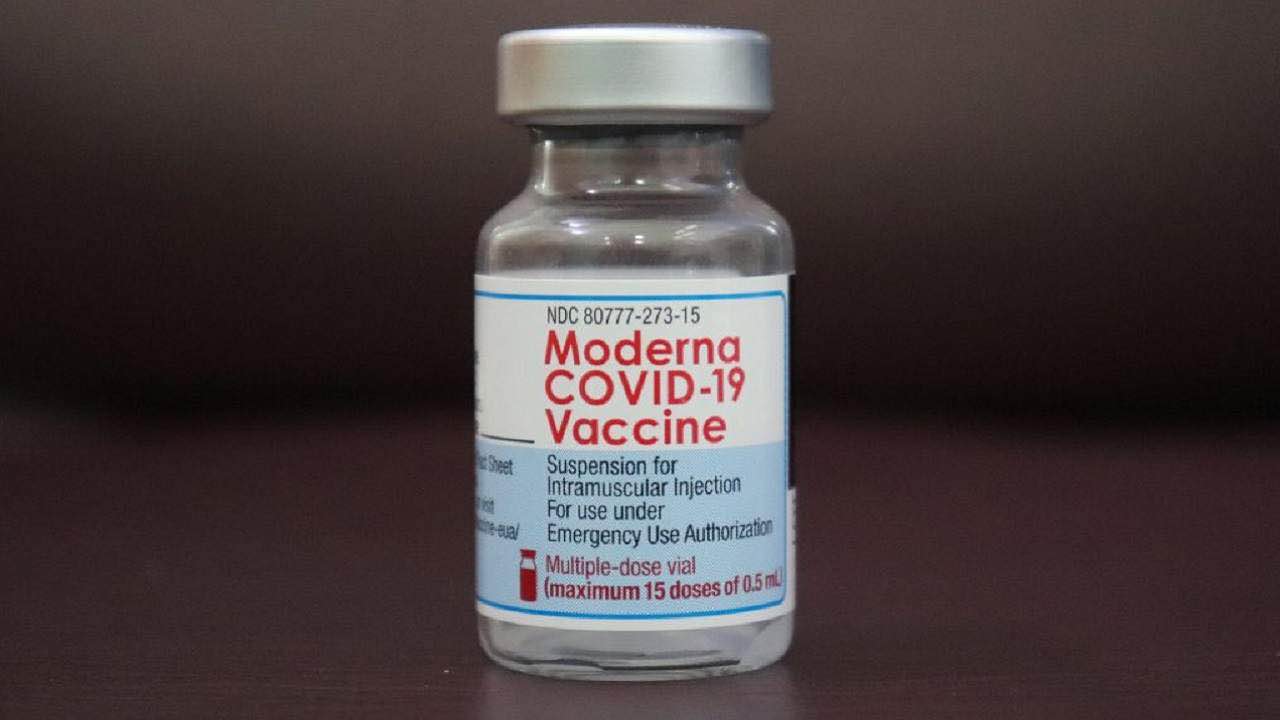
Foto Pixabay | mufidpwt
L’azienda farmaceutica Moderna ha chiesto oggi agli enti regolatori statunitensi di autorizzare l’uso di dosi ridotte del suo vaccino anti Covid-19 per i bambini con meno di sei anni. Lo riporta l’Associated Press.
Stando ai dati inviati alla Food and Drug Administration, secondo la società due dosi ridotte del suo vaccino fornirebbero una protezione sufficiente per i minori in età prescolare. Negli Usa anche la “rivale” Pfizer sta conducendo degli studi sulla protezione offerta da tre dosi del siero sviluppato con BioNTech nei più piccoli. Nei mesi scorsi, i test avevano infatti rivelato che due dosi non erano abbastanza efficaci.
Vaccino Covid ai bambini: sarà per tutti o solo per i più fragili?
In caso di via libera da parte dell’Fda, toccherebbe poi ai Cdc – i Centers for Disease Control and Prevention – stabilire la platea di somministrazione. Ovvero, stabilire se il vaccino di Moderna sia necessario per tutti i bambini under 6 oppure solo per quelli più fragili e dunque più esposti a un rischio sanitario maggiore. Le dosi su cui si basa la richiesta di autorizzazione sono pari a un quarto di quelle indicate per gli adulti.
A seguire saranno poi le altre agenzie del farmaco (come l’Ema in Europa) a valutare se seguire l’esempio americano. Come ricorda l’Ap, il virus si è dimostrato più aggressivo negli adulti rispetto ai bambini. Dall’inizio della pandemia, comunque, negli Usa sono morti di Covid 475 bambini con meno di cinque anni. Si è inoltre registrato un incremento dei contagi durante la fase acuta della diffusione della variante Omicron.
LEGGI ANCHE: Omicron 4 e 5, tutto quello che sappiamo sulle due nuove sottovarianti
Moderna sta infine valutando un vaccino booster bivalente (mRna-1273.214) che combina il vaccino attualmente autorizzato anche come richiamo con un candidato booster specifico per le varianti Omicron. I risultati iniziali dello studio, di fase clinica 2-3, sono attesi nel secondo trimestre dell’anno. Questo booster bivalente “rimane il nostro candidato principale per una dose di richiamo” da somministrare “nell’emisfero settentrionale nell’autunno 2022”, ha dichiarato il Ceo della casa farmaceutica, Stéphane Bancel.
